电位滴定法与永停滴定法
实验过程中,滴定终点的判断尤为重要。电位滴定法与永停滴定法,凭借客观精准的终点指示能力,成为容量分析中的“黄金标准”。本文将系统拆解两种方法的原理、装置、操作要点及维护技巧掌握两种滴定方法。”
一、方法原理
传统指示剂滴定法依赖肉眼观察颜色变化,易受主观经验、光线条件影响,而电位滴定法与永停滴定法通过电极系统将化学变化转化为电信号,实现终点的客观判定。
1.电位滴定法:电位突跃
电位滴定法采用指示电极+参比电极的组合系统:
指示电极的电位随被测离子浓度变化而波动(如玻璃电极响应H⁺浓度);
参比电极提供稳定不变的基准电位(如饱和甘汞电极);
滴定终点时,被测离子浓度急剧变化引发指示电极电位“突增”或“突减”,形成可量化的突跃点。
这种方法适用于酸碱中和(水溶液/非水溶液)、沉淀反应、氧化还原等多种反应类型,尤其在有色溶液、浑浊体系中优势显著。
2.永停滴定法:电流突变
永停滴定法使用两支相同的铂电极,通过低电压(通常50mV)下的电流变化判断终点:
滴定前若电极极化,溶液中几乎无电流通过;
终点时滴定液微量过剩使电极去极化,电流突然增大且稳定不变;
特殊反应中也会出现“去极化→极化”的逆转,表现为电流从有到无。
该方法在重氮化反应、水分测定中应用广泛,其电流突变的直观性堪称“滴定界的红绿灯”。
二、仪器组成与配置
两类方法的仪器装置既有共性,又各具特色,选择合适的设备是实验成功的基础。
电极系统选型
不同反应类型需搭配特定电极,以下为药典推荐组合:
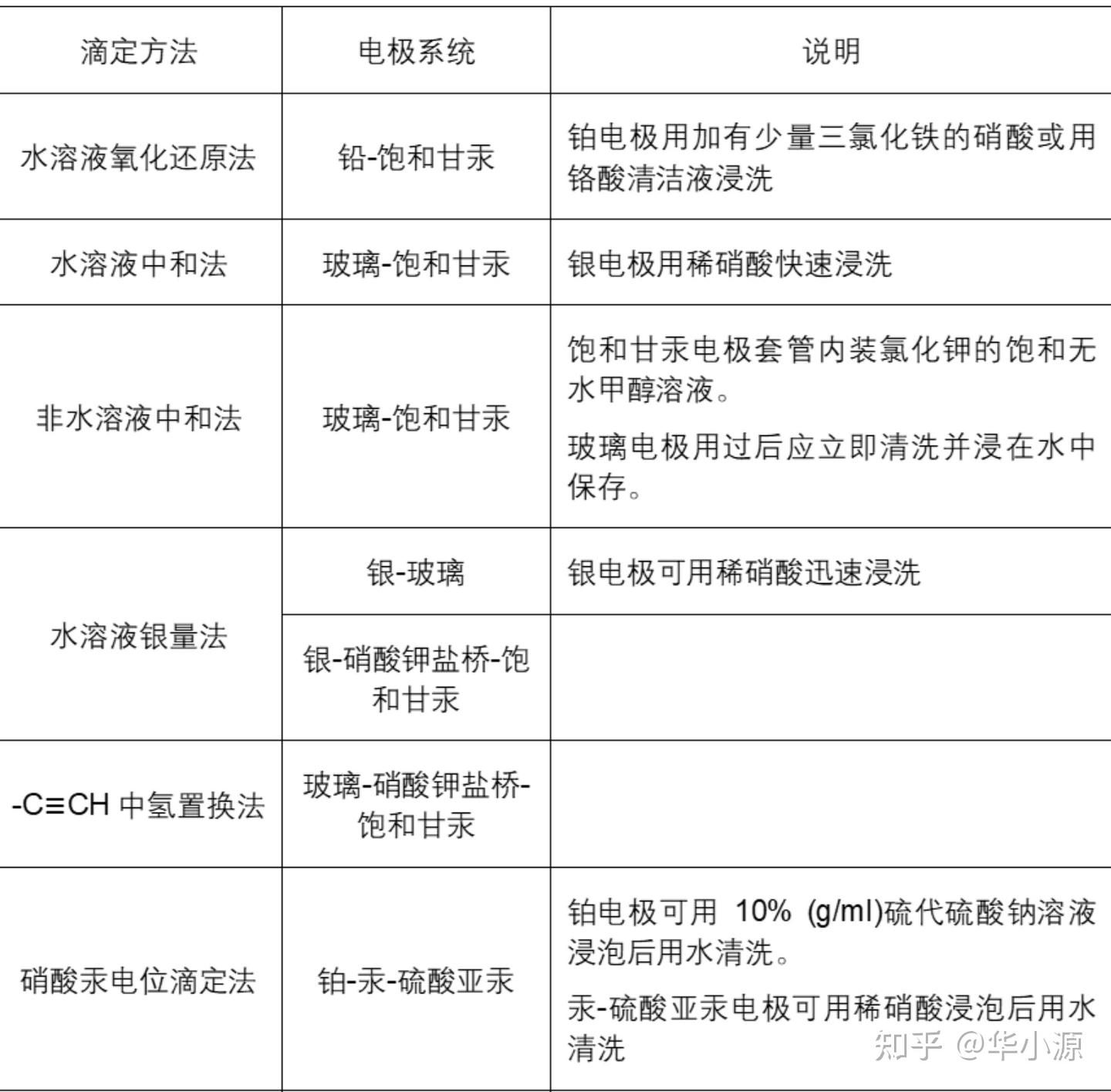
电极维护要点:玻璃电极使用后需立即浸于水中;铂电极避免触碰硬物,定期用10%硫代硫酸钠溶液处理。
三、操作步骤
1.电位滴定法标准步骤
(1)样品准备:精密称取供试品,加溶剂溶解后置于电磁搅拌器上。
(2)电极安装:浸入指示电极与参比电极,确保电极不接触搅拌子。
(3)滴定操作:
- 初始阶段:每次加入较大量滴定液,记录体积与电位。
- 近终点时:减小滴加量(通常0.1-0.2ml/次),精确记录。
- 终点后:继续滴加3-5次,获取完整滴定曲线。
(4)终点判定方法:
- 作图法:以电位(E)为纵坐标,体积(V)为横坐标,取曲线拐点为终点。
- 一阶导数法:计算ΔE/ΔV,极值对应的体积为终点。
- 二阶导数法:通过Δ²E/ΔV²=0的点计算终点,公式如下:
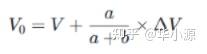
(a为过零前二级微商绝对值,b为过零后绝对值,V为a对应的体积)
其中二阶导数法因精度最高,成为药典首选方法。
2.永停滴定法操作步骤
以重氮化法为例:
(1)样品处理:供试品加水40ml与盐酸15ml溶解,加溴化钾2g。
(2)电极插入:铂电极浸入溶液,滴定管尖端插入液面下2/3处。
(3)滴定控制:
快速滴定至近终点,提出滴定管尖端,淋洗后缓缓滴加。
观察电流计指针:突然偏转且不再回复即为终点。
(4)水分测定特殊要求:
调节初始电流至5-10μA;
终点判定:电流突增至50-150μA并持续数分钟不回落。
四、影响结果准确性的因素
1.仪器因素
- 电位计精度:应定期校准,确保误差≤±0.1mV;
- 电流计灵敏度:选择不当会导致终点误判(如重氮化法需高灵敏度);
- 搅拌速度:过快易产生气泡附着电极,过慢则反应不均。
2.操作因素
- 滴定速度:近终点时需缓慢滴加,避免错过突跃点;
- 电极浸入深度:需保持一致,避免液面波动影响读数;
- 温度影响:非水溶液滴定中,温度变化超过10℃需重新标定滴定液浓度。
3.计算校正公式
当高氯酸滴定液标定与样品测定温度差异超过10℃,需按以下公式校正:
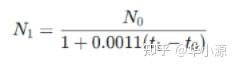
(0.0011为冰醋酸膨胀系数,t₀为标定温度,t₁为测定温度)
五应用拓展
1.药物含量测定实例
阿司匹林肠溶片(中和法):用玻璃-甘汞电极系统,电位滴定法确定终点;
盐酸普鲁卡因(重氮化法):永停滴定法指示终点,精度优于外指示剂法;
有机碱氢卤酸盐:加醋酸汞试液消除干扰后,用高氯酸非水滴定。
2.水分测定第一法(卡尔费休法)
采用永停滴定原理,当样品中水分完全反应后,过量的碘使电极去极化,电流突增为终点信号,适用于多数有机药物的微量水分测定。
六
常见问题与解决方案
1.电位突跃不明显
原因:样品浓度过低、滴定剂浓度不当;
对策:浓缩样品或更换更高浓度滴定液,增加搅拌速度。
2.永停滴定无电流变化
原因:铂电极极化失效、电路接触不良;
对策:用铬酸清洁液活化电极,检查接线是否松动。
3.电极响应迟缓
原因:电极老化、溶液离子强度低;
对策:更换新电极,加入支持电解质(如硝酸钾)。
4.终点判定重现性差
原因:搅拌速度不稳定、滴定速度过快;
对策:使用恒温搅拌器,近终点时采用半滴操作法。






